-
Dispositivos para liberação de fármacos (Drug Delivery)
O Sistema ou dispositivo de liberação de fármaco (drug delivery devices – DDDs) é definido como uma formulação ou um dispositivo que permite a liberação de uma substância terapêutica no corpo de uma maneira controlada ou retardada em um local específico, o que aumenta a sua eficácia e segurança. Existem dois tipos principais de dispositivos para liberação controlada de fármacos: dispositivos do tipo monolíticos e resarvatório.
Nos dispositivos do tipo monolíticos o fármaco encontra-se distribuído homogeneamente ou solubilizado na matriz polimérica. Quando as matrizes poliméricas são hidrofílicas e não inertes, o processo é regulado por intumescimento do polímero, difusão e erosão da matriz. Os dispositivos monolíticos podem ser empregados em diversas formas farmacêuticas como comprimidos, cápsulas gelatinosas, grânulos, sistemas trans-dérmicos, implantes, entre outros.
Sistemas do tipo reservatório são dispositivos no qual o fármaco (sólido ou líquido) encontra-se em um núcleo isolado do meio externo por uma capa ou membrana, geralmente polimérica. Neste tipo de sistema a concentração de saturação do fármaco no interior do dispositivo é essencial para manter um gradiente de concentração constante através da membrana. O mecanismo de transporte do fármaco através da membrana é controlado por difusão e depende da solubilidade do fármaco, da afinidade química entre o fármaco e a matriz polimérica, do caráter hidrofílico da matriz polimérica e da microestrutura e porosidade da matriz polimérica.
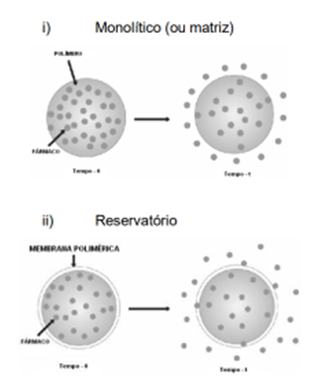
Dispositivos para liberação controlada de fármacos disponíveis comercialmente compostos por partes de polímeros e blendas poliméricas são fabricados por diferentes processos como evaporação de solventes, vazamento, extrusão, moldagem por compressão, moldagem por injeção e outros. Na fabricação de dispositivos porosos existem processos que podem ser aplicados com maior facilidade. Dentre as técnicas de fabricação rápida em camadas, a sinterização seletiva a laser (Selective Laser Sintering – SLS), permite a fabricação de dispositivos porosos. A sinterização seletiva a laser baseia-se na sinterização de materiais particulados, através do calor fornecido por um feixe de laser infravermelho, para formar um objeto sólido pela deposição de camadas.


O processo de SLS apresenta ainda algumas facilidades para a fabricação de dispositivos com controle de microestrutura, porosidade e função, tais como: o controle localizado da composição e dos parâmetros de processo, bem como uma grande liberdade na construção de “geometrias complexas”.



Seguem o link de artigos sobre o assunto produzidos pelo autor
PCL/Ibuprofen Implants Fabricated by Selective Laser Sintering for Orbital Repair
Sobre o autor

Prof. Dr. Gean Vitor Salmoria
Possui graduação e mestrado pela Universidade Federal de Santa Catarina (1993). Obteve o doutorado em Processamento por Microondas no Institut Nacional Polytechnique de Toulouse-France (2000). Atualmente é Professor e Orientador de Doutorado no Departamento de Engenharia Mecânica da Universidade Federal de Santa Catarina. Atua na área de Engenharia Mecânica, com ênfase em Processos de Fabricação com Materiais Poliméricos, pesquisando os seguintes temas: Processos de fabricação utilizando microondas e lasers infravermelho e ultravioleta, processos e materiais para manufatura aditiva e fabricação rápida, projeto e fabricação de ferramental rapido, moldagem por injeção e extrusão de produtos poliméricos para industria eletro-eletrônica, automobilística, aeroespacial e biomedica . Faz parte dos Professores Coordenadores do Nucleo de Moldagem e Manufatura Aditiva (NIMMA) e do Laboratório de Engenharia Biomecânica do Hospital Universitário (LEBM). Consultor industrial e associado a ABNT-ISO na área de materiais para implantes médicos. (www.engenhariabiomecanica.ufsc.br)
-
Ácido Hialurônico
O que é?
O ácido hialurônico (AH) pode ser classificado como um biopolímero glicosaminoglicano solúvel em água formado a partir da junção do ácido glucurônico e da N-acetilglucosamina (BERNARDES et al., 2018). É sintetizado pelos sinoviócitos do tipo B presentes na membrana sinovial. No líquido sinovial as moléculas de AH se entrelaçam formando uma solução cuja função é lubrificar a articulação, além de ser um suporte mecânico e amortecedor de choques (REZENDE e CAMPOS, 2012).

Qual a importância da compreensão do ácido hialurônico e suas aplicações?
A osteoartrite (OA) é uma doença multifatorial onde ocorre a degeneração do tecido cartilaginoso e ósseo, promovendo um processo inflamatório intenso e necrose celular. Afeta as articulações, principalmente quadril, joelhos, mãos e pés; prejudicando seriamente a qualidade de vida da população adulta e principalmente a idosa, onde a doença tem maior prevalência (REZENDE et al., 2013). Em alguns casos pacientes afetados pela osteoartrite perdem a capacidade de trabalhar justamente pelas dores articulares causadas por essa degeneração (COIMBRA et al., 2004).

As causas da OA são diversas, porém estudos indicam que obesidade, fatores genéticos, uso excessivo, trauma, idade e gênero são determinantes para o processo de lesão na articulação, desencadeamento o processo patológico da OA (REZENDE et al., 2013). De acordo com Rezende et al. (2013), durante a OA ocorre também a inflamação da membrana sinovial nas regiões em que articulação já está danificada pela doença, sendo encontradas no líquido sinovial proteinases e citocinas inflamatórias que são capazes de acelerar o processo de degeneração articular.
Geralmente, para o tratamento da OA eram utilizadas medidas farmacológicas como analgésicos, anti-inflamatórios não hormonais e drogas modificadoras da osteoartrite (DMDOA) junto com medidas não-farmacológicas, como fisioterapia e acupuntura, sendo a última comprovada no alívio da dor dos pacientes (REZENDE e CAMPOS, 2012). Porém, dentro das medidas farmacológicas, os analgésicos não conseguem impedir o avanço da doença, os anti-inflamatórios possuem inúmeros efeitos colaterais e o único grupo de medicamentos que realmente consegue reverter, desacelerar ou estabilizar o avanço da doença são as DMDOA (REZENDE et al., 2013).
Dentro das DMDOA utilizam-se medicamentos como a diacereína, condroitina e glicosamina. A eficácia dessas substâncias é amplamente discutida e, em estudos recentes, acredita-se que a associação da glicosamina com a condroitina pode prejudicar a absorção da glicosamina no organismo, afetando sua ação terapêutica (REZENDE et al., 2013).
Concomitante às DMDOA existe a viscossuplementação que consiste em injetar ácido hialurônico nas articulações diartrodiais, onde há interface de dois ossos, de modo que esta interface seja preenchida pelo líquido sinovial. Segundo Oliveira et al. (2019) esse método era utilizado para tratar cavalos de corrida que sofriam de artrite traumática e logo após foi adaptado para humanos.

A injeção de ácido hialurônico faz com que ele, no líquido sinovial, diminua a inflamação atuando como modulador dos sinoviócitos que secretam as citocinas e outras enzimas inflamatórias além de também estimular sinoviócitos do tipo B a secretarem mais ácido hialurônico. Adicionalmente, restaura a viscosidade, melhora a distribuição de forças e reduz a pressão de contato na articulação. Como coadjuvante, atua junto um anti-inflamatório corticóide que garante o alívio da dor e que diminui mais rapidamente o efeito inflamatório (REZENDE e CAMPOS, 2012).
Em estudos referentes a resultados clínicos, a viscossuplementação apresenta bons resultados, sendo que a melhora ocorre entre a 5ª e a 13ª semana de tratamento em pacientes com osteoartrite. A maioria das aplicações ocorrem para tratamento da OA no joelho, porém também pode ser utilizada para tratar a doença no quadril, ombros, tornozelos, cotovelos, mãos e os pés (REZENDE e CAMPOS, 2012).
Em resumo, o ácido hialurônico apresenta uma boa relação custo-efetividade em relação ao número de suas aplicações no tratamento de OA, o que aumenta a sua importância econômica na área médica (REZENDE e CAMPOS, 2012).
Para pacientes que mesmo com a viscossuplementação ainda apresentam dor, instabilidade e com a funcionalidade da articulação comprometida, ou seja, não obtiveram um progresso satisfatório no tratamento, recomenda-se que o próximo passo seja a artroplastia.
Sobre o Autor
 Gabriel Padilha é técnico em química formada pelo IFSC e atualmente está cursando Graduação em Farmácia na UFSC. Gabriel é estagiário no Laboratório de Engenharia Biomecânica desde 2021, onde é responsável pela condução de ensaios de liberação de fármacos.
Gabriel Padilha é técnico em química formada pelo IFSC e atualmente está cursando Graduação em Farmácia na UFSC. Gabriel é estagiário no Laboratório de Engenharia Biomecânica desde 2021, onde é responsável pela condução de ensaios de liberação de fármacos.Referências
BERNARDES, I. N.; COLI, B. A.; MACHADO, M. G.; OZOLINS, B. C.; SILVÉRIO, F. R.; VILELA, C. A.; ASSIS, I. B. de; PEREIRA, L. Preenchimento com ácido hialurônico – Revisão de Literatura. Revista Saúde em Foco, 2018, v. 10, p. 603-618. Disponível em: <https://portal.unisepe.com.br/unifia/wp-content/uploads/sites/10001/2018/07/070_PREENCHIMENTO_COM_%C3%81CIDO_HIALUR%C3%94NICO.pdf>. Acesso em: 27 de janeiro de 2022.
MESTRINER, L. A.; FILHO, J. L. Artroplastia total do joelho em pacientes com artrite reumática e osteoartrose. Revista Brasileira de Ortopedia, 1993, vol. 28, n. 4, p. 211-218. Disponível em: <https://rbo.org.br/detalhes/869/pt-BR/artroplastia-total-do-joelho-em-artrite-reumatoide-e-osteoartrose>. Acesso em: 24 de maio de 2022.
OLIVEIRA, L. E. A. de; BRÍGIDO, J. A.; SALDANHA, A. D. D. Efeitos da infiltração de ácido hialurônico no tratamento das desordens internas da articulação
Temporomandibular. Brazilian Journal of Pain, São Paulo, 2019, vol. 2, n. 2, p. 182-186. Disponível em:<https://www.scielo.br/j/brjp/a/hzTD5rLyksJz6bnSXjfZrbt/abstract/?lang=pt#>. Acesso em: 28 de janeiro de 2022.
REZENDE, M. U. de; CAMPOS, G. C. de; PAILO, A. F. Conceitos atuais em osteoartrite. Acta Ortopédica Brasileira, 2013, vol. 21, n. 2, p. 120-122. Disponível em: <https://www.scielo.br/j/aob/a/wSLfqHbYjphBVLdqBCMdP4z/?lang=pt>. Acesso em: 28 de janeiro de 2022.
REZENDE, M. U. de; CAMPOS, G. C. Viscosuplementação. Revista Brasileira de Ortopedia, 2012, vol. 47, n. 2, p. 160-164. Disponível em: <https://www.scielo.br/j/rbort/a/Y83fscJZp76cCk6Gk5Jm8Dw/?lang=pt>. Acesso em: 28 de janeiro de 2022.
-
Tecnologia dos Stents e sua evolução
Stents
Os stents são pequenos dispositivos tubulares, utilizados principalmente como tratamento de doença coronariana, que são inseridos em artérias, veias ou em outros canais bloqueados, com objetivo de restaurar o fluxo sanguíneo desses vasos danificados. Portanto, esses implantes devem ser capazes de não sofrerem deformação em segmentos que apresentam calcificação e obstruções e de resistir as variadas forças do ciclo cardíaco.
Esses tubos são formados por malhas metálicas de aço inoxidável, platina-cromo ou cobalto-cromo, as quais podem apresentar revestimento polimérico. O intuito do revestimento é utilizar fármacos que auxiliem no impedimento do crescimento de tecidos e na cicatrização da parede do vaso sanguíneo, os quais podem causar novos estreitamentos, devido a coágulos de sangue no local onde o stent foi implantado. Estes stents, os stents farmacológicos, são utilizados em 95% dos casos, pois apresentam melhores resultados a longo prazo. Além disso, os stents farmacológicos também reduzem as taxas de uma possível nova intervenção cirúrgica e, principalmente, o risco do paciente desenvolver trombose. [1, 2,3, 4]

Stents bioabsorvíveis
Stents bioabsorvíveis, ou suportes vasculares bioabsorvíveis (BVS), também são uma solução para tratamento de doença coronariana e são utilizados em casos mais gerais, quando o vaso não é muito pequeno e tortuoso. Esses dispositivos possuem o mesmo princípio inicial dos stents com fármacos, são implantados no vaso obstruído para retomar o fluxo sanguíneo no local e liberar o fármaco.
A absorção do stent pelo organismo começa após seis meses de sua inserção, são transformados em água e dióxido de carbono devido ao ciclo de Krebs celular, e termina em até dois anos, mantendo o vaso desobstruído e com o formato do dispositivo, mesmo após seu desaparecimento, diminuindo a chance da necessidade de uma nova operação e riscos de infarto e trombose [2,3,5]
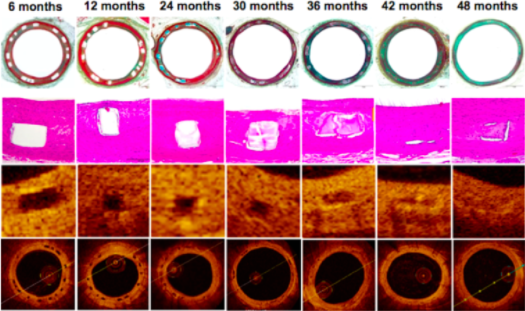
Evolução da absorção do stent bioabsorvivel no organismo [6].
Angioplastia
Angioplastia com stent é um procedimento médico realizado com o objetivo de restaurar o fluxo sanguíneo por meio da introdução de uma malha no interior do vaso obstruído.
Inicialmente, os procedimentos de angioplastia não contavam com a presença de stents, era utilizado balões simples e muitos casos resultaram em re-estreitamento do vaso sanguíneo. A primeira cirurgia de implante de stent convencional ocorreu em março de 1986, por Jacques Puel, na França. Ulrich Sigwart meses depois, na Suiça, realizou um procedimento que revolucionou o conceito e aplicação final do stent coronário, conhecido como stent endoluminal [7]. O primeiro stent foi aprovado pela FDA em 1987 e desenvolvido por Schatz e colaboradores [8].
A inserção de um stent é feita através de um cateter, introduzido na virilha ou no punho do paciente, o qual é guiado até o vaso sanguíneo bloqueado. Um balão localizado no cateter se expande e posiciona o stent na parede da artéria, retomando o fluxo sanguíneo no local [1].
A evolução dos stents
Primeira Geração
A primeira geração de stents, os stents de metal, eram compostos pela liga de aço inoxidável 316L SS, pois apresentavam excelentes propriedades mecânicas e altas resistências a corrosão. Embora essa liga apresentar bons resultados, impedindo o recuo da artéria após seu implante, como o ferro é o elemento mais presente na liga, esses stents possuíam alto poder de absorção de raios X e baixa compatibilidade a ressonância magnética. Uma tentativa de melhorar esse problema com os raios X ocorreu, adicionando ouro a liga, mas isso só aumentou o índice de reestenose e mortalidade que essa geração de stents apresentou. [9]

Estruturas dos Stents da primeira geração [11]
Ligas de cromo-cobalto
A liga cromo-cobalto apresenta uma melhor radio-opacidade e resistência radial em relação a liga anterior devido a melhores propriedades mecânicas, como modulo de elasticidade e resistência ao escoamento, e maior densidade. Essas propriedades possibilitaram stents com hastes mais finas, melhorando a flexibilidade, diâmetro interno e diminuindo lesões na parede do vaso e risco de reestenose. Também estão disponíveis stents compostos por ligas de platina-cromo, com maior radio-opacidade [9].
Stents com fármaco
Os primeiros stents com fármaco utilizavam PEVA como revestimento polimérico. Atualmente, polímeros mais biocompatíveis, como fluoreto de polivinilideno, são utilizados e ainda assim, inflamações precoces ocorrem. Revestimentos com polímeros biodegradáveis, ácido polilático, também são uma opção no mercado, mas não apresentam grandes diferenças nos resultados [9].
Estudos foram realizados com intuito de remover o revestimento polimérico e adicionar o fármaco diretamente na estrutura metálica do stent. Embora o polímero ajude na diminuição do risco de trombose e possíveis sangramentos, sua remoção é uma alternativa para diminuir a exposição do endotélio aos excessivos processos inflamatórios que ocorrem após a introdução do stent. Modificações na porosidade e na estrutura cristalina do metal ou, agregar o fármaco a partir de ligações covalentes ou nanopartículas ocorreram para que o polímero pudesse ser removido e as doses dos fármacos continuassem a serem controladas [10].
Materiais bioabsorvíveis
A utilização de materiais totalmente bioabsorviveis em stents é atual e podem ser formados tanto por materiais poliméricos quanto por metais, que possam ser absorvidos pelo organismo. Melhores propriedades mecânicas e biocompatibilidade estão sendo observadas em dispositivos bioabsorvidos a base de ligas de magnésio e possivelmente em ligas de zinco [11].
Estudos estão sendo desenvolvidos com relação aos stents bioabsorvíveis para que consigam abranger casos de aplicação em veias mais finas, pois esse tipo de dispositivo apresentas hastes maiores que os stents metálicos, impossibilitando sua utilização em casos mais sensíveis. E também, com relação a sua utilização em casos de pacientes mais jovens e com outros problemas de saúde [5]. Inovações estão sendo estudadas relacionadas ao design dos stents, para seu melhor uso em lesões de bifurcação, e novos avanços tecnológicos nos stents carotídeos [7]. O desenvolvimento de um stent metálico com fármaco com propriedade anti-reestenose e, de um material de revestimento capaz de criar uma fina camada natural quando inserido na parede da artéria são caminhos de futuro desses implantes [12].
Sobre a autora

Sophia Mannes é graduanda do curso de engenharia de materiais na Universidade Federal de Santa Catarina e desde 2021 trabalha com análise de implantes poliméricos no LEBm. Recentemente tem se aproximado da área de pesquisa de stents junto ao Núcleo de Inovação em Moldagem e Manufatura Aditiva, coordenado pelo Prof. Dr. Gean Vitor Salmoria.
Mais informações sobre Sophia acesse:
https://www.linkedin.com/in/sophia-mannes-361265192/Referências
[1] https://www.paho.org/pt/topicos/doencas-cardiovasculares
[2] https://cardiopapers.com.br/stents-bioabsorviveis-por-que-para-quem-quando-evitar/
[3] https://www.hcor.com.br/materia/stent-bioabsorvivel-reduz-chances-de-novas-obstrucoes-nas-arterias/
[4] https://www.bhf.org.uk/informationsupport/heart-matters-magazine/medical/how-do-stents-work#:~:text=What%20is%20a%20stent%20made,could%20cause%20re%2Dnarrowing).
[5] https://www.hcor.com.br/imprensa/noticias/hcor-realiza-o-primeiro-implante-de-stent-bioabsorvivel/#:~:text=Sousa%20realizou%20em%20todo%20o,cardiologia%20brasileira%2C%20com%20repercuss%C3%A3o%20mundial.
[6] https://cardiopapers.com.br/stents-bioabsorviveis-por-que-para-quem-quando-evitar/
[7] https://www.healio.com/news/cardiology/20120225/stents-at-25-years-a-revolution-in-revascularization
[8] https://academic.oup.com/bmb/article/106/1/193/321394
[9] https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6025441/
[10] https://socesp.org.br/revista/assets/upload/revista/7974972351543860416pdfenSTENTS%20FARMACOL%C3%93GICOS-%20ESTADO%20ATUAL_REVISTA%20SOCESP%20V28%20N1_INGLES.pdf
[11] https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7202450/
[12] https://www.webmd.com/heart-disease/stents-types-and-uses
-
PARTICIPAÇÃO DO LEBm E CNAEx NO CONGRESSO DA ORTHOPAEDIC RESEARCH SOCIETY 2022
As equipes do LEBm e CNAEx, representados pelo seu coordenador de engenharia Prof. Carlos Rodrigo de Mello Roesle e a gerente de pesquisa Dra. Patricia Ortega Cubillos, participaram do congresso anual da Orthopaedic Research Society 2022 , em Tampa nos Estados Unidos.
O grupo formado pelo LEBm, CNAEx e Grante, em conjuntom apresentaram seis trabalhos desenvolvidos dentro de suas estruturas e auxílio de parceiros.

Na imagem, à esquerda o Prof. Rodrigo Roesler, à sua direita , Dra. Patricia Ortega, Prof. Fanccelo e o Dr. José Leonardo Rocha
Abaixo seguem os links para download dos trabalhos apresentados.
A new Outlook on the acetabular liners damage assessment and performance
A retrieval study of fretting corrosion analysis at the stem head and stem-cement interface of total hip arthroplasty
Biomechanical analysis of Inside out continous menical sutures vs. Traditional meniscal repair A pilot Study
Influence of the glenoid labrum on the glenohumeral joint stability by a finite element shoulde model
Macroscopic Analysis of Fixed-bearing Posterior Stabilized TKA Retrieved Inserts
Wear performance of hip prostheis tested under the same test conditions, same hip simulator, and simultaneosly -
Quanto tempo dura uma prótese de Silicone e quais suas chances de ruptura?
Quanto tempo dura uma prótese de Silicone?
É difícil precisar quanto tempo dura uma prótese de silicone, pois a prótese não deixa de funcionar iminentemente após o prazo determinado. Com o passar do tempo, porém, as interações químicas e forças cíclicas sobre a prótese podem degradar suas propriedades e aumentar a possibilidade de ruptura ou efeitos indesejados. A FDA recomenda que a remoção ou troca seja feita em 10 anos[1], mas há diversos relatos de mulheres que prolongaram esse período sem casos de complicações.
Quais as chances de ruptura da prótese?
A chances de ruptura são relacionadas à quantidade de incidências de ruptura dentro de um grupo amostral. A ruptura ocorre, principalmente, por danificação da prótese no momento de implantação (perfuração pela agulha do ponto ou outro objeto perfurante), encapsulamento da prótese, ou impactos como um acidente de carro ou um impacto recorrente em uma atividade física como judô[2].

A)Vista transversal da membrana, dano causado por uma agulha, B) visão transversal da membrana, dano causado por um corte de bisturi e C) Dano causado pela encapsulamento da prótese.
Fonte: N. Handel, M. E. Garcia, and R. Wixtrom, “Breast implant rupture: causes, incidence, clinical impact, and management,” Plast. Reconstr. Surg., vol. 132, no. 5, pp. 1128–1137, 2013, doi: 10.1097/PRS.0b013e3182a4c243.
De acordo com a FDA, cerca de 20% das rupturas ocorrem entre 8 e 10 anos[1]. Dentro da revisão bibliográfica realizada pelo LEBm foram encontrados diversos índices para chances de ruptura da prótese, dependendo da marca, do modelo e do tempo de uso. Está bem estabelecido que, com o passar do tempo, a prótese de silicone tem mais probabilidade de ruptura[3].
A tabela abaixo apresenta estudos de avaliação de segurança das próteses após determinado tempo decorrido.
Fabricante
Tempo in-vivo (anos)
Forma Probabilidade de ruptura (%) Probabilidade de contratura capsular (%) Probabilidade reoperação (%) Nome do estudo A 5 Redonda 1,8 9 23,8 Five-year follow-up data from the U.S. clinical trial for Sientra’s U.S. Food and Drug Administration-approved Silimed® brand round and shaped implants with high-strength silicone gel[4] A 8 Redonda 4,6 11,8 28,3 Eight-Year Follow-Up Data from the U.S. Clinical Trial for Sientra’s FDA-Approved Round and Shaped Implants with High-Strength Cohesive Silicone Gel[5] A 10 Redonda 8,6 13,5 31,5 Ten-year Core Study Data for Sientra’s Food and Drug Administration-Approved Round and Shaped Breast Implants with Cohesive Silicone Gel[6] B 8 Redonda e shaped 0,9 8,5 6 Eight-Year Safety Data for Round and Anatomical Silicone Gel Breast Implants[7] B 10 Redonda e Shaped 3,8 11,5 13,3 Ten-Year Safety Data for Eurosilicone’s Round and Anatomical Silicone Gel Breast Implants[8] C 6 Shaped 2,1 2,4 18,1 Mentor Contour Profile Gel implants: clinical outcomes at 6 years[9] C 6 Redonda 1,1 9,8 19,4 Safety and Effectiveness of Mentor’s MemoryGel Implants at 6 Years[10] C 10 Não menciona 24,2 12,1 25,5 MemoryGel Breast Implants: Final Safety and Efficacy Results after 10 Years of Follow-Up[11] D 3 Não menciona 1 4,8 Style 410 highly cohesive silicone breast implant core study results at 3 years[12] D 6 Não menciona 3,8 4,6 Style 410 highly cohesive silicone breast implant core study results at 6 years D 10 Não menciona 7,7 18,9 28 Natrelle Round Silicone Breast Implants: Core Study Results at 10 Years[13] E 6 Não menciona 3,5 17,5 32 Inamed Silicone Breast Implant Core Study Results at 6 Years[14] F 7 Não menciona 5 3 An extended 7-year review of textured breast implants for primary breast augmentation: Allergan® versus Mentor[15] F 10 Redonda 9,3 Silicone breast implant rupture: a review[16] F 10 Shaped 17,7 Silicone breast implant rupture: a review[16] G 4 Não menciona 0 2,3 BellaGel breast implant: 4-year results of a prospective cohort study[17] G 6 Não menciona 1,15 2,3 BellaGel breast implant: 6-Year results of a prospective cohort study

Desde 1962, quando a primeira prótese foi implantada, diversos aprimoramentos foram realizados. Nos dias atuais é difícil de encontrar um paciente com a primeira geração e segunda geração de próteses. As próteses dessas gerações tinham mais chances de ruptura. Em um estudo realizado em 2003 por Holmich et al[3] intitulado “Incidence of Silicone Breast Implant Rupture”, no qual próteses de primeira e segunda geração ainda poderiam ser encontradas, próteses após 20 anos tinham até 35% de chance de ruptura. Ainda dentre as de primeira geração avaliadas, 28% romperam, de segunda geração, 14% e terceira geração, 3,6%. Além disso o gel dessas próteses era menos coeso, ocasionando o vazamento de gel para os tecidos.

A)Prótese de primeira geração com sinais de vazamento, B) prótese de segunda geração com sinais de ruptura e C) ruptura por intracapsulamento da prótese.
Fonte: C. Hillard, J. D. Fowler, R. Barta, and B. Cunningham, “Silicone breast implant rupture: A review,” Gland Surg., vol. 6, no. 2, pp. 163–168, Apr. 2017, doi: 10.21037/gs.2016.09.12.
Hoje, em caso de ruptura da membrana, o gel é produzido para que não vaze para fora. Próteses mais modernas de sexta, sétima e oitava geração, conhecidas com gummy bear breast implants, não são mais preenchidas com gel, mas compostas de um sólido gelatinoso[18]. Fizemos um post falando sobre a geração e próteses e suas evoluções, que pode ser conferido aqui

Se você ou sua empresa tem interesse em melhorar a segurança e a eficácia de próteses mamárias de silicone, entre em contato com o Laboratório de Engenharia Biomecânica para realização de cooperação técnico-científica, o Laboratório é acreditado pela Cgcre de acordo com a ABNT NBR ISO/IEC 17025, sob número CRL 1223. Entre em contato conosco clicando aqui
Confira nosso escopo atualizado em: http://www.inmetro.gov.br/laboratorios/rble/detalhe_laboratorio.asp?nom_apelido=UFSC%2FLEBM#“
Referências
[1] FDA, “Breast Implants-Certain Labeling Recommendations to Improve Patient Communication Guidance for Industry and Food and Drug Administration Staff Preface Public Comment,” 2020, Accessed: Oct. 19, 2021. [Online]. Available: https://www.regulations.gov.
[2] N. Handel, M. E. Garcia, and R. Wixtrom, “Breast implant rupture: causes, incidence, clinical impact, and management,” Plast. Reconstr. Surg., vol. 132, no. 5, pp. 1128–1137, 2013, doi: 10.1097/PRS.0b013e3182a4c243.
[3] L. R. Hölmich et al., “Incidence of silicone breast implant rupture,” Arch. Surg., vol. 138, no. 7, pp. 801–806, 2003, doi: 10.1001/archsurg.138.7.801.
[4] S. WG et al., “Five-year follow-up data from the U.S. clinical trial for Sientra’s U.S. Food and Drug Administration-approved Silimed® brand round and shaped implants with high-strength silicone gel,” Plast. Reconstr. Surg., vol. 130, no. 5, pp. 973–981, Nov. 2012, doi: 10.1097/PRS.0B013E31826B7D2F.
[5] W. G. Stevens, J. Harrington, K. Alizadeh, D. Broadway, K. Zeidler, and T. B. Godinez, “Eight-Year Follow-Up Data from the U.S. Clinical Trial for Sientra’s FDA-Approved Round and Shaped Implants with High-Strength Cohesive Silicone Gel,” Aesthetic Surg. J., vol. 35, no. suppl_1, pp. S3–S10, May 2015, doi: 10.1093/ASJ/SJV020.
[6] S. WG, C. MB, A. K, Z. KR, H. JL, and d’Incelli RC, “Ten-year Core Study Data for Sientra’s Food and Drug Administration-Approved Round and Shaped Breast Implants with Cohesive Silicone Gel,” Plast. Reconstr. Surg., vol. 141, no. 4S Sientra Shaped and Round Cohesive Gel Implants, pp. 7S-19S, Apr. 2018, doi: 10.1097/PRS.0000000000004350.
[7] D. F, P. P, B. MH, and S. S, “Eight-Year Safety Data for Round and Anatomical Silicone Gel Breast Implants,” Aesthetic Surg. J., vol. 38, no. 2, pp. 151–161, Feb. 2018, doi: 10.1093/ASJ/SJX117.
[8] D. F, P. P, B. MH, B. E, and S. S, “Ten-Year Safety Data for Eurosilicone’s Round and Anatomical Silicone Gel Breast Implants,” Aesthetic Surg. journal. Open forum, vol. 1, no. 2, Apr. 2019, doi: 10.1093/ASJOF/OJZ012.
[9] H. DC, M. MM, C. DA, G. ME, and P. CA, “Mentor Contour Profile Gel implants: clinical outcomes at 6 years,” Plast. Reconstr. Surg., vol. 129, no. 6, pp. 1381–1391, 2012, doi: 10.1097/PRS.0B013E31824ECBF0.
[10] C. B and M. J, “Safety and effectiveness of Mentor’s MemoryGel implants at 6 years,” Aesthetic Plast. Surg., vol. 33, no. 3, pp. 440–444, 2009, doi: 10.1007/S00266-009-9364-6.
[11] C. DA, C. MB, W. RN, E. MM, and C. JW, “MemoryGel Breast Implants: Final Safety and Efficacy Results after 10 Years of Follow-Up.,” Plast. Reconstr. Surg., vol. 147, no. 3, pp. 556–566, Mar. 2021, doi: 10.1097/PRS.0000000000007635.
[12] B. BP, V. N. BW, M. DK, S. A, and M. GP, “Style 410 highly cohesive silicone breast implant core study results at 3 years,” Plast. Reconstr. Surg., vol. 120, no. 7 Suppl 1, Dec. 2007, doi: 10.1097/01.PRS.0000286666.29101.11.
[13] S. L. Spear and D. K. Murphy, “Natrelle round silicone breast implants: Core study results at 10 years,” Plast. Reconstr. Surg., vol. 133, no. 6, pp. 1354–1361, 2014, doi: 10.1097/PRS.0000000000000021.
[14] S. SL, M. DK, S. A, and W. PS, “Inamed silicone breast implant core study results at 6 years,” Plast. Reconstr. Surg., vol. 120, no. 7 Suppl 1, Dec. 2007, doi: 10.1097/01.PRS.0000286580.93214.DF.
[15] S. V. Martin, W. Ho, and K. Kha, “An extended 7-year review of textured breast implants for primary breast augmentation: Allergan ® versus Mentor ®,” Ann. Breast Surg., vol. 3, no. 0, pp. 14–14, Jul. 2019, doi: 10.21037/ABS.2019.06.01.
[16] C. Hillard, J. D. Fowler, R. Barta, and B. Cunningham, “Silicone breast implant rupture: A review,” Gland Surg., vol. 6, no. 2, pp. 163–168, Apr. 2017, doi: 10.21037/gs.2016.09.12.
[17] H. J, J. JH, B. SI, and H. CY, “BellaGel breast implant: 4-year results of a prospective cohort study,” J. Plast. Surg. Hand Surg., vol. 53, no. 4, pp. 232–239, Jul. 2019, doi: 10.1080/2000656X.2019.1583572.
[18] “7th generation breast implants: softer, safer, less ripply!” https://www.drkarenhorton.com/dr-hortons-blog/7th-generation-breast-implants-softer-safer/ (accessed Oct. 13, 2021).
-
A EVOLUÇÃO DAS PRÓTESES MAMÁRIAS
Em 1895, o Dr.Czerny relatou o primeiro reconstrução de mama. Nessa situação um linfoma do tronco foi transplantado para a mama de uma paciente após uma mastectomia parcial. Durante os próximos 50 anos, os cirurgiões tentaram implantar vários materiais na mama, como marfim, vidro, bolas, borracha, cartilagem, lã , guta-percha, chips de polietileno e esponjas, mas sem sucesso.[1][2].

Fonte: https://allthatsinteresting.com/weird-history-of-breast-implants?utm_campaign=twitterpdtyc&utm_source=twitter&utm_medium=social
Em 2010, a Cirurgia de implantes mamários é a cirurgia mais popular dos Estados Unidos, sendo 318 mil cirurgias realizadas, dentre 62% usaram próteses mamárias de silicone. Desde de 1962, nos estados unidos foram criados aproximadamente 240 tipos diferentes de próteses por 10 fabricantes diferentes e com cerca de 8300 modelos de tamanhos, formatos, espessuras, texturas, dentre outros aspectos diferentes[3].
Primeira Geração de próteses de silicone
Nos anos 60 começaram testes com membranas a partir de silicone e em 1962, Cronin e Gerow relataram o uso do primeiro implante mamário de silicone gel. Este era composto de um gel de silicone viscoso contido dentro de uma espessa membrana de silicone. Esses dispositivos protéticos de dois componentes projetados com uma membrana de elastômero de silicone preenchida com um material de enchimento estável, consistindo de solução salina ou gel de silicone. As próteses até então eram feitas por um invólucro de elastômero de Silicone com uma espessura maior, superfície lisa e preenchida com gel de silicone. As rupturas eram raras, no entanto complicações por encapsulamento da prótese eram comuns, por questões inflamatórias ou movimentação da prótese[1][2].

Fonte:https://allthatsinteresting.com/weird-history-of-breast-implants?utm_campaign=twitterpdtyc&utm_source=twitter&utm_medium=social
Segunda geração de próteses de silicone
Em meados da década de 1970 surgiu a segunda geração de próteses mamárias com membranas mais finas e preenchimento menos viscoso. O principal objetivo dessas próteses era assemelhar-se mais a realidade, mas também reduzir as contraturas capsulares. Infelizmente, não apenas as taxas de contratura capsular permaneceram inalteradas, como esses dispositivos frágeis estavam mais sujeitos à ruptura[1].

Fonte: https://www.drglicksman.com/breast-surgery/evolution-implants/
Terceira geração de próteses mamárias
A década de 80, viu avanços significativos na tecnologia de silicone. Membranas mais fortes reduziram a quantidade de óleo de silicone que “vazava” para os tecidos adjacentes, em caso de ruptura. O conteúdo do gel tornou-se mais viscoso e coeso.

Fonte: http://plennacirurgiaplastica.com.br/tipos-de-implantes-mamarios-protese-de-mama/
Ainda na década de 80, as membranas de superfície texturizada tornaram-se disponíveis. Pareceu-se que isso reduzia as taxas de contratura capsular. Nesse contexto o revestimento de poliuretano de implantes ganhou popularidade. A redução da contratura capsular observada com dispositivos revestidos com poliuretano foi atribuída à sua estrutura de células abertas, que permitiu o crescimento do tecido para dentro e evitou uma deposição circunferencial regular de colágeno[4].

Fonte: www.thepmfajournal.com/features/post/perspectives-on-polyurethane-covered-breast-implants
Também na década de 80 se popularizam as próteses com duplo lúmen, essas compostas por uma prótese de gel e em seu interior um outra prótese, essa preenchida com solução salina permitindo um ajuste final com a prótese já dentro do corpo. Apesar de prover um permitindo um aspecto mais natural, o procedimento não era possível para todo os pacientes, além de a prótese ser mais complexa para se confeccionar e possuíam mais chances de ruptura[1].

Fonte: www.24-7pressrelease.com/press-release/203222/inventor-of-first-adjustable-cosmetic-breast-implant-spectra-presents-invention-in-brazil
Devido a diversos incidentes, em 1992 com próteses da Dow Corning, a FDA manda retirar todos os implantes preenchidos com gel de silicone do mercado para estudos mais aprofundados do produto. Vários países europeus seguem o exemplo[1].
A retirada das próteses preenchidas com gel, do mercado, permitiu que as próteses preenchidas com solução salina dominassem o mercado, até 2006 quando a FDA retira a restrição e a implementação da quarta e quinta geração de próteses no mercado[5].
Quarta e quinta geração de próteses mamámarias
A publicidade adversa observada na década de 1990 resultou em padrões de fabricação mais rígidos. Os implantes atuais da quarta e quinta gerações são essencialmente dispositivos refinados de terceira geração. Essas próteses incluem produtos de gel coesivo com maior reticulação. O gel resultante é muito mais rígido e mantém sua forma mesmo quando cortado, portanto, capaz de controlar a propagação do conteúdo do gel em caso de ruptura da membrana. No entanto, são necessárias incisões mamárias maiores para acomodar esses implantes menos flexíveis. Em um esforço para reduzir o vazamento de gel de dispositivos preenchidos com silicone, grupos fenil ou trifluoropropil são ligados à membrana para diminuir a permeabilidade da membrana ao gel de silicone. Estas membranas de baixo vazamento com revestimento de barreira são características dos implantes atuais de terceira, quarta e quinta geração.

Fonte: https://www.clarin.com/salud/implantes-mamarios_0_SJHiQnjPXg.html
Sexta, sétima e oitava geração
Essa geração é voltada para próteses subgrandular, ou seja por cima do musculo. Esse tipo de prótese possuem um gel mais macio e adaptável, o que resulta em um aspecto mais natural ao ficar de pé e deitado, com movimento e maciez mais parecidos com o tecido mamário natural. O gel é mais macio possibilita a inserção da prótese por meio de uma incisão menor. Além disso, a superfície nano-texturizada da prótese, tem uma textura mais fina em comparação com as próteses mamárias convencionais.

Fonte: www.breastaugmentation101.com/breast-implant-singapore-philippines-asian-countries/
Em um estudo com essa nova geração, os envolvidos afirmaram que 84,6% experimentaram menos complicações gerais e 76,9% confirmaram taxas reduzidas de contratura capsular com esses dispositivos. No geral, 84,6% dos especialistas preferiram selecionar implantes da nova geração aos anteriores para obter uma aparência mais natural. Além disso, 92,3% dos especialistas concordaram que a prótese, devido ao sua tecnologia inovadora, reduz o risco de linfoma anaplásico de células grandes[6].
Outra diferença é que até então as próteses de silicone disponíveis eram preenchidos com aproximadamente 85% da sua capacidade e, portanto, estavam sujeitos a leves “ondulações” (ou “enrugamento”), com dobras do implante visíveis através da pele. Isso ocorreria principalmente em mulheres com perfil atlético, muito magras ou em casos de reconstrução mamária em que o implante era colocado na parte superior do músculo – também conhecida como posição “pré-peitoral”. A ondulação sempre foi mais severa em implantes salinos, pois eles fluem como água, em oposição ao silicone, que é um gel mais viscoso[7].

Fonte: www.drkarenhorton.com/dr-hortons-blog/7th-generation-breast-implants-softer-safer/
A sétima geração trás uma prótese, também com preenchimento de 96%de sua cavidade, mas com um gel ainda mais coeso. Mas diferentemente do que era chamados os “gummybears implants” com gel altamente coeso, que produziam grandes cicatrizes e tinham um perfil mais rígido, essa nova geração é possui as mesmas propriedades estruturais, porém muito mais macia e permite cicatrizes menores[7].
A oitava geração apresenta as mesmas características da sétima e sexta geração, porém possui um perfil mais macio.
Sobre o Autor
Lucas Kurth de Azambuja é Mestre e Engenheiro de Materiais, formado pela UFSC, especializado na área de polímeros. Também realizou intercâmbio para França na École Nationale d’ingénieurs de Saint-Étienne e estagiou na École de Mines de Saint Étinne. Desde 2017, Lucas é bolsista no Laboratório de Engenharia Biomecânica, onde realizou seu trabalho de conclusão de curso focado no estudo de degradação de implantes mamários. Posteriormente realizou sua dissertação, também no laboratório, focado na análise de insertos acetabulares após uso em in vivo. Hoje é resposável pela execução das análises poliméricas do laboratório, além de colaborar no projeto do Centro Nacional de Explante.
Lucas possuí dois trabalhos publicados sobre o estudo de próteses mamárias
- de Mello Gindri, Izabelle, et al. “Evaluation of invitro degradation of commercially available breast implants.” Polymer Testing 79 (2019): 106033
- de Mello Gindri, Izabelle, et al. “Influence of Breast Implant Surface Finishing on Physicochemical and Mechanical Properties before and after Extreme Degradation Studies.” International journal of biomaterials 2021 (2021).
Referências
[1] V. Vinci et al., “The evolution of breast prostheses,” Breast J., vol. 26, no. 9, pp. 1801–1804, Sep. 2020, doi: 10.1111/TBJ.13954.
[2] E. Kelly, “The Surprisingly Weird History Of Breast Implants,” Ati, 2016. https://allthatsinteresting.com/weird-history-of-breast-implants (accessed Oct. 11, 2021).
[3] I. Pitanguy, N. Amorim, A. Ferreira, and R. Berger, “Análise das trocas de implantes mamários nos últimos cinco anos na Clínica Ivo Pitanguy,” Rev. Bras. Cir. Plástica, vol. 25, no. 4, pp. 668–674, 1AD.
[4] N. Castel, T. Soon-Sutton, P. Deptula, A. Flaherty, and D. Parsa, “Polyurethane-Coated Breast Implants Revisited: A 30-Year Follow-Up,” 2015, doi: 10.5999/aps.2015.42.2.186.
[5] C. for D. and R. Health, “Breast Implants – Regulatory History of Breast Implants in the U.S.,” Accessed: Jan. 15, 2018. [Online]. Available: https://www.fda.gov/MedicalDevices/ProductsandMedicalProcedures/ImplantsandProsthetics/BreastImplants/ucm064461.htm.
[6] M. Sforza et al., “Expert Consensus on the Use of a New Bioengineered, Cell-Friendly, Smooth Surface Breast Implant,” Aesthetic Surg. J., vol. 39, pp. S95–S102, Apr. 2019, doi: 10.1093/ASJ/SJZ054.
[7] “7th generation breast implants: softer, safer, less ripply!” https://www.drkarenhorton.com/dr-hortons-blog/7th-generation-breast-implants-softer-safer/ (accessed Oct. 13, 2021).
-
“COMO” E “DO QUE” SÃO FEITAS AS PRÓTESES MAMÁRIAS.
A prótese de silicone é formada por uma membrana de silicone reticulado e preenchido com gel de silicone.

O silicone
O silicone ou polidimetilsiloxano é um polímero cuja cadeia principal é formada por moléculas de silício e oxigênio com grupamentos radicas metílicos.

Na temperatura ambiente o silicone é considerado um polímero líquido, pois seu ponto de fusão, ou seja, ponto o qual o material passa da fase sólida para a fase líquida, é de -40°C. Para se obter esse polímero em um estado sólido na temperatura ambiente, opta-se por uma técnica de reticulação, essa técnica cria “nós de ancoragem” conferindo ao material uma estrutura tridimensional.

As primeiras gerações de próteses eram preenchidas com silicone líquido, porém, quando havia um vazamento na membrana, o líquido escoava muito facilmente para fora da prótese. Sendo assim, as gerações seguintes passaram a ser preenchidas com silicone gel, que tem mais dificuldade de escoamento em caso de ruptura.
Desde 1962, vários implantes foram desenvolvidos por diferentes fabricantes, totalizando cerca de 8000 tipos diferentes entre tamanhos, formas, texturas e modos de preenchimento.
Tamanhos
Hoje no mercado é possível encontrar próteses de silicone de 150ml até 600ml.

Formas
Formas, as próteses tem diversas formas para melhor se encaixam com cada estrutura de corpo. A forma da prótese vai depender do molde que a membrana foi confeccionada.
As próteses podem ter forma de gota, cônica, arredondada, podem possuir perfil baixo ou moderado.

Textura
Inicialmente as próteses eram todas lisas, porém essas tinham maiores chances de gerar contraturas capsulares ou de se movimentarem. As próteses texturizadas aumentam a área de adesão com o tecido, assim impedindo a movimentação. Ainda, mais recentemente voltaram a ser produzidas as próteses de silicone recobertas com espuma de poliuretano.

Preenchimento
Na maioria dos casos, nas próteses mais modernas, essas são preenchidos com gel de silicone.

Apesar disso, outras próteses podem ter duplo lúmen, uma cavidade preenchida com gel de silicone e uma cavidade mais externa preenchida com solução salina. Esse tipo de prótese pode ser ajustado na cirurgia, para melhor se ajustar ao corpo e não ficar presa a medidas fixas como na de preenchimento apenas com gel.

Como são produzidas essas próteses?
Inicialmente é necessário um molde, esse é imerso em silicone líquido. Após a imersão o molde é levado a um forno o qual ocorre a reticulação. Esse ciclo ocorre para quantas camadas que se pretende obter. Após finalizada essa etapa, a membrana está constituída no molde, essa então é removida e preenchida com gel silicone. Após preenchimento, a região de abertura é selada com uma membrana chamada de “patch”. Após a produção essa prótese ainda irá passar por diversos processos de qualidade, aos quais abordaremos em outra postagem.

Para próteses texturizadas o processo é um pouco diferente, segue o mesmo processo de imersão em gel de silicone, reticulação e preenchimento, porém dentre as camadas da membrana de silicone, o molde é mergulhado em areia (quartzo), reticulado e o areia removida em seguida. O espaço antes ocupados pela areia irá formar uma textura no implante.

Referências
[1] I. Pitanguy, N. Amorim, A. Ferreira, and R. Berger, “Análise das trocas de implantes mamários nos últimos cinco anos na Clínica Ivo Pitanguy,” Rev. Bras. Cir. Plástica, vol. 25, no. 4, pp. 668–674, 1AD, Accessed: Apr. 02, 2018. [Online]. Available: http://www.rbcp.org.br/details/763/analise-das-trocas-de-implantes-mamarios-nos-ultimos-cinco-anos-na-clinica-ivo-pitanguy.
[2] S. Barr and A. Bayat, “Breast Implant Surface Development: Perspectives on Development and Manufacture,” Aesthetic Surg. J., vol. 31, no. 1, pp. 56–67, Jan. 2011, doi: 10.1177/1090820X10390921.
[3] M. Grigg, S. Bondurant, V. L. Ernster, and R. Herdman, “Information for Women about the Safety of Silicone Breast Implants,” 2000. Accessed: Aug. 28, 2019. [Online]. Available: http://www.nap.edu/catalog/9618.html.
Sobre o Autor.

M.e. Eng. Lucas Kurth de Azambuja
Lucas Kurth de Azambuja é Mestre e Engenheiro de Materiais, formado pela UFSC, especializado na área de polímeros. Também realizou intercâmbio para França na École Nationale d’ingénieurs de Saint-Étienne e estagiou na École de Mines de Saint Étinne. Desde 2017, Lucas é bolsista no Laboratório de Engenharia Biomecânica, onde realizou seu trabalho de conclusão de curso focado no estudo de degradação de implantes mamários. Posteriormente realizou sua dissertação, também no laboratório, focado na análise de insertos acetabulares após uso em in vivo. Hoje é resposável pela execução das análises poliméricas do laboratório, além de colaborar no projeto do Centro Nacional de Explante.
Lucas possuí dois trabalhos publicados sobre o estudo de próteses mamárias
- de Mello Gindri, Izabelle, et al. “Evaluation of invitro degradation of commercially available breast implants.” Polymer Testing 79 (2019): 106033
- de Mello Gindri, Izabelle, et al. “Influence of Breast Implant Surface Finishing on Physicochemical and Mechanical Properties before and after Extreme Degradation Studies.” International journal of biomaterials 2021 (2021).
-
OUTUBRO ROSA – LEBm

O Laboratório de Engenharia Biomecânica neste mês presta o seu apoio ao Outubro Rosa.
Aos que não sabem, o Outubro Rosa é um movimento internacional de conscientização para o controle do câncer de mama. A data é celebrada anualmente e tem como objetivo compartilhar informações e promover a conscientização sobre a doença.
No Brasil, o câncer de mama é o tipo de câncer mais incidente em mulheres de todas as regiões, após o câncer de pele não melanoma. Em 2021, estima-se que ocorrerão 66.280 casos novos da doença, o que equivale a uma taxa de incidência de 43,74 casos por 100.000 mulheres (INCA, 2020). A incidência do câncer de mama tende a crescer progressivamente a partir dos 40 anos, assim como a mortalidade por essa neoplasia (INCA, 2019).
Em muitos casos, as mulheres necessitam reconstruir a mama ou retirá-la. de acordo com o TABNET, sistema de gestão de procedimentos da saúde, de 2008 até 2021 foram realizadas pelo SUS cerca de 97.763 mastectomias radical com linfadenectomia axilar em oncologia, que consiste na retirada da mama e glândulas mamária, além disso, o SUS também realizou 18.355 plásticas mamaria reconstrutiva pós mastectomia com implante de prótese de mama.
Mas qual a relação do LEBm com o assunto?
Em 2010, após escândalos com a empresa PIP implants, o LEBm auxiliou na regulamentação do mercado de implantes de silicone no Brasil e hoje é acreditado pela Cgcre de acordo com a ABNT NBR ISO/IEC 17025, sob número CRL 1223, para análises de implantes de silicone.
Visto a experiência do laboratório, o LEBm irá realizar uma série de postagem sobre assuntos relacionados a próteses mamárias neste mês, como: do que são feitas, como são feitas, histórico de evolução das próteses, quais as chances de ruptura, dentre outros assuntos, com o intuito de trazer informações de utilidade pública sobre o tema para o nosso público.
Acompanhe o laboratório ao longo deste mês.
-
Visita do Dr. José Leonardo Rocha de Faria. M.D. , M.Sc. para ensaios de técnicas sutura meniscal contínua e inside-out
Reafirmando o compromisso do LEBm/HU-UFSC para a melhoria das técnicas cirúrgicas e da qualidade dos dispositivos médicos implantáveis, foram realizados nos dia 15, 16 e 17 de setembro os experimentos biomecânicos para avaliação da técnicas de sutura de menisco desenvolvidas pelo Dr. José Leonardo Rocha de Faria. M.D. , M.Sc.. (INTO/MS). Da equipe do LEBm, o Dr. Leonardo pode contar com o auxílio do Prof. Dr. Carlos Rodrigo de Mello Roesler e do M.Sc. Eng. Arthur Paiva. Além disso os ensaios ainda contaram com a presença do Prof. Dr. Rodrigo Salim, da USP de Ribeirão Preto, a aluna de medicina Mariana Radulski e a equipe da empresa Síntegra Surgical Science representados pelo Bruno e pelo Caio.

Da direita para esquerda: Mariana Radulski, Dr. Leornardo Farias, Dr. Rodrigo Salim, MSc. Eng. Arthur Santos, Dr. Eng. Rodriigo Roesler, Bruno, Dr. Ari Moré. Abaixo Caio
Dr. José Leonardo Rocha de Faria é ortopedista e traumatologista especializado em cirurgia do joelho. Fez sua formação em ortopedia e cirurgia do joelho no Instituto Nacional de Traumatologia e Ortopedia – INTO/MS, junto ao serviço de cirurgia do joelho, o qual realiza cerca de 30 a 40 cirurgias do joelho semanalmente. Mais informações sobre o Dr. José Leonardo Rocha de Faria, acesso aqui!
Dr. José Leonardo Rocha de Farias
O projeto em parceria com o LEBm reside na análise biomecânica comparativa de dois tipos de sutura meniscal: continua x inside-out.A técnica da sutura continua foi desenvolvida pelo Dr. José Leonardo Rocha de Farias e grupo de pesquisa envolvendo o INTO/MS, LEBm/HU-UFSC, Twin Cities Orthopaedics, University of Minnesota Medical School, Faculdade de Ciências Médicas da Universidade Estadual do Rio de Janeiro e Hospital das Clinicas de Ribeirão Preto.
Agora o projeto comparou a sutura menical contínua e inside-out em 58 meniscos, de joelhos porcinos, para comparação da técnica.
Os ensaios ainda contaram com a presença do Dr. Rodrigo Salim, orientador de Doutorado do Dr. Leonardo e uma refêrencia na ortopedia de joelho e mdicina do esporte. Mais infomrações sobre o Dr. Salim, acesse aqui!

Os meniscos suturados foram testados em uma máquina universal Zwick/Roell Z2.5 TN, nas estruturas do LEBm.

Abaixo podemos visualizar um vídeo de um menisco surturado sendo testado
A descrição da técnica pode ser vista no artigo científico publicado na Arthroscopy Techniques em jun/2021:
“Continuous Meniscal Suture in Radial Meniscal Tear: The Hourglass Technique”.O Dr. Leonardo aind apossui outros 3 asrtigos científicos na área:
Sutura Meniscal Contínua do Joelho, Nova Técnica para sutura do menisco – Continuous Meniscal Suture of The Knee.
José Leonardo Rocha de Faria, Douglas Mello Pavão, Alfredo Villardi, Eduardo Branco de Sousa, João Matheus Guimarães, José Maurício de Morais Carmo and Alan de Paula Mozella.
https://www.arthroscopytechniques.org/article/S2212-6287(20)30045-1/fulltextVertical Continuous Meniscal Suture Technique.
José Leonardo Rocha de Faria, Douglas Mello Pavão, Raphael Serra Cruz, Eduardo Branco de Sousa, João Matheus Guimarães, Marcelo Costa de Oliveira Campos and Alan de Paula Mozella.
https://www.arthroscopytechniques.org/article/S2212-6287(20)30134-1/fulltextOutside-in Continuous Meniscal Suture Technique of The Knee
José Leonardo Rocha de Faria, Douglas Mello Pavão, Vitor Barion Castro de Padua, Eduardo Branco de Sousa, João Matheus Guimarães, Berliet Assad Gomes, Alan de Paula Mozell
https://www.arthroscopytechniques.org/article/S2212-6287(20)30164-X/fulltext




